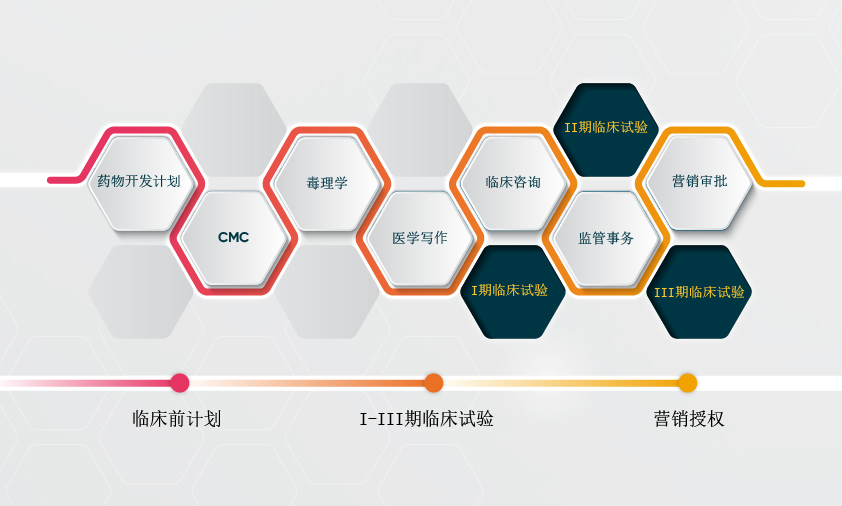
药物研发战略
合适的研发战略对于加快药物开发具有至关重要的意义。随着生物技术公司投资项目的复杂化和全球化,监管规划不容忽视和小觑,它涵盖临床方案设计、非临床试验计划、生产工艺等多个方面。诺为泰提供优秀监管服务,在复杂及动态的研究环境中加速药物开发进程。
核心监管服务
- 监管差距评估和战略
- 非临床毒理学研究的设计和审查
- 撰写研究员手册(IB)
- 国际递交,包括IND、DMF、NDA、BLA和组合产品
- 会议和简报包,包括A型、B型和C型会议、科学建议
- 快速通道和孤儿药资格认定
- 美国代理服务
- 机构生物安全委员会和转基因药物应用
核心医疗服务
- 医学写作
- 临床试验设计
- 医学监测
- 药物警戒
从开始、研发到批准,诺为泰药物研发咨询将始终为您保驾护航。