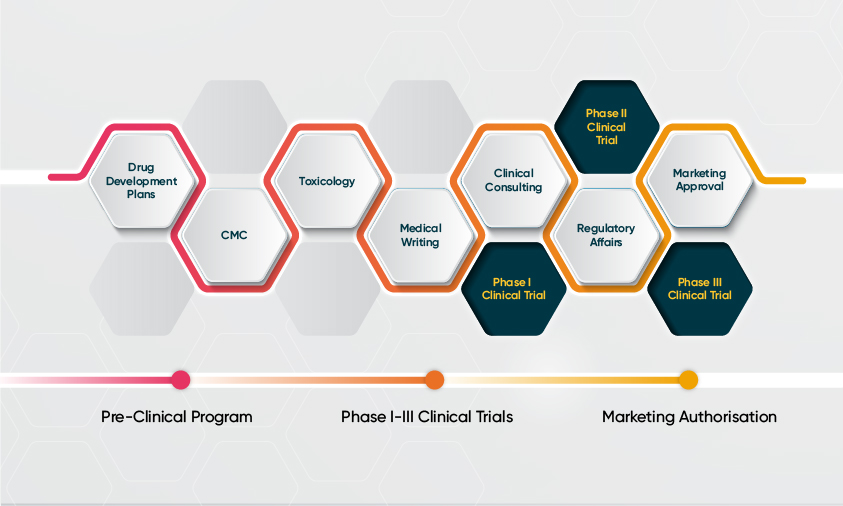
노보텍의 의료 및 규제 컨설팅 팀은 완전한 범위의 전임상, 규제 업무 지원, 의료 및 약물감시 컨설팅 서비스를 제공합니다.
노보텍의 의료 서비스 팀은 각 임상시험에서 지속적인 운영 성공의 토대가 되는 학제적 접근법, 메디컬 라이팅, 약물감시, 의료 모니터링 및 중앙 연구소 서비스를 제공합니다.
노보텍의 의료 서비스는 고객사의 임상시험계획서별 요구 사항에 따라 최적화되며 표적 임상 파라미터 제공을 목표로 하는 동시에 의학 및 안전성 감독과 규제 관련 지원 모두를 제공합니다.
노보텍은 안전성 모니터링 및 증례 처리에 최신 약물감시 플랫폼인 Oracle ARGUS를 활용합니다.
임상 개발 전략
올바른 개발 전략은 귀사 약물 및 회사의 미래에 매우 중요합니다. 생명공학 기업들이 보다 복잡한 글로벌 프로그램에 투자하면서 생명공학 임상시험의뢰자들은 동유럽 및 아시아 태평양과 같은 미국 외 지역에서 임상시험을 수행하는 것을 더 많이 고려하고 있습니다. 신중하게 설계된 임상시험계획서를 이용하는 것을 포함해 최신 임상 개발 전략에 대한 투자도 증가하고 있습니다. 여기에는 적응형 무작위배정을 활용한 다중군 다단계 설계가 포함됩니다. 임상시험 설계에 대한 효율적 접근 방식은 의약품 개발 비용 상승을 억제하는 데 가장 큰 영향을 줄 것으로 보입니다.
임상 규제
노보텍은 최고 수준의 규제 서비스를 제공하여 복잡하고 역동적인 연구 환경에서 신속한 의약품 개발이 이루어지도록 지원합니다.
HREC/IRB 신청서 작성은 특화된 규제 업무입니다. 노보텍은 1996년 규제 업무 컨설팅 업체로 설립되어, 제약 및 생명공학 산업에 규제 업무 서비스를 제공하는 데 강점을 보유하고 있습니다. 노보텍의 상급 규제 업무 전문가는 윤리위원회 승인 및 규제 프로세스를 관리하여, 효율적으로 적시에 모든 연구가 시작될 수 있도록 최선을 다합니다.
규제 업무과 관련한 이러한 심층적인 경험은 아시아 태평양 지역의 주요 기관을 포괄합니다.
BioDesk의 핵심 서비스
- 임상 및 제품 개발 계획의 개발.
- 임상 또는 승인을 위한 고객사의 제품 GMP 준수 및 준비 지원.
- 인간대상 연구와 판매 승인 지원 차원의 클라이언트의 GLP 준수 독성 연구 설계 및 조율.
- 사전 IND, IND, CTX, 희귀 의약품 지정(ODD) 소아과 시험 계획(PIP)에서 시판 승인 신청(MAA)에 이르는 모든 유형의 신청서 작성.
- 공급업체 조달 및 관리.
- 임상시험계획서, 임상시험자 자료집 및 시판 승인 신청(MAA)에 필요한 일반 기술 문서의 모든 모듈 설계와 작성.














